马斯克亲测的“减肥神药”国内申批?司美格鲁肽新适应证上市申请获受理
阿輝 2023-06-04 13:47 2650 浏览 0 评论
特斯拉CEO马斯克亲测过的“减肥神药”在国内的上市步伐或又进一步。
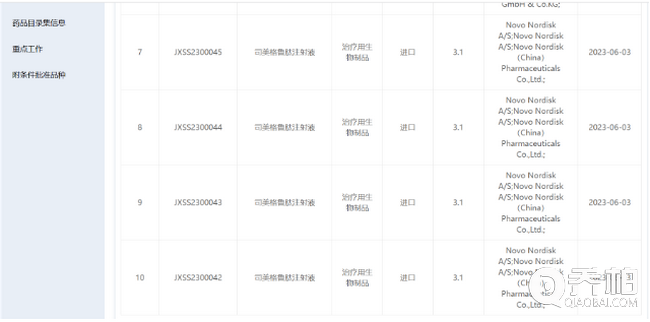
6月3日,国家药监局药审中心(CDE)官网显示,全球胰岛素巨头诺和诺德的司美格鲁肽注射液的新适应证上市申请已获得受理。受理品种信息并未披露该适应证的具体内容,但业内普遍认为,该适应证大概率与减重相关。
根据“临床试验默示许可”信息显示,此前诺和诺德(Novo Nordisk A/S)的司美格鲁肽注射液临床试验适应症:作为低热量饮食和增加体力活动的辅助治疗,用于初始体重指数(BMI)≥24.0且<28.0 kg/m2(超重)且伴有至少1种体重相关合并症,或BMI≥28.0且<30.0 kg/m2(肥胖)有或无体重相关合并症的成人患者体重管理。
司美格鲁肽的减肥适应证也为诺和诺德贡献了极佳的业绩。2022年财报显示,该药销售额61.88亿丹麦克朗(约合人民币63亿元),同比增长346%。2023年第一季度,Wegovy销售额达45.63亿丹麦克朗(约合人民币46.5亿元),同比增长225%。
司美格鲁肽注射液属于GLP-1(胰高血糖素样肽-1)受体激动剂,最早用于二型糖尿病治疗。2021年6月,该药在美国获批用于成人肥胖症,商品名为Wegovy。此次获批依据的临床试验结果显示,在每周1次皮下注射司美格鲁肽治疗12周后,2.4mg剂量组肥胖或超重患者的平均体重减轻6%左右;68周时减重17%至18%。
2022年10月,马斯克曾在社交媒体提到,自己一个月内减重18斤,方法包括节食和Wegovy,后者正是司美格鲁肽注射液的商品名。马斯克的亲测有效,也让司美格鲁肽注射液成功出圈。减重数据不错,加上每周仅需一针,司美格鲁肽被部分人视为“减肥神药”或“瘦身针”。
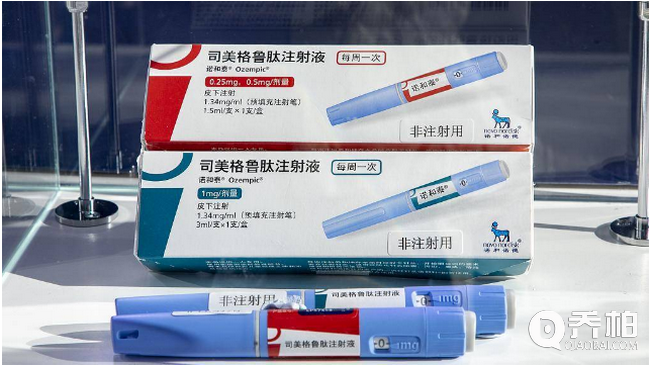
在国内,司美格鲁肽于2021年4月首次在中国获批上市,用于辅助饮食和运动以改善2型糖尿病(T2DM)患者的血糖控制,商品名为诺和泰。现实生活中,不少人主动“超适应证”使用该药用于减重,一度有糖尿病患者反映司美格鲁肽在部分医院出现缺货情况。
司美格鲁肽注射液说明书
药品简介
司美格鲁肽以天然人GLP-1分子为基础,通过替换第8位(丙氨酸→α-氨基丁酸)和第34位氨基酸(赖氨酸→精氨酸),同时在第26位赖氨酸通过间隔基连接C18脂肪二酸侧链。经过对人GLP-1分子的改造,司美格鲁肽实现了可抵抗二肽基肽酶4(DPP-4)降解、与白蛋白紧密结合,体内半衰期显著延长,实现每周给药1次,同时保留了高达94%的GLP-1氨基酸序列同源性,具有较好的安全性。
2017年12月,美国食品与药物管理局(FDA)批准司美格鲁肽注射液上市,用于成人2型糖尿病患者的血糖控制。
2020年1月,获FDA批准,用于降低伴有心血管疾病的2型糖尿病成人患者的主要心血管不良事件风险。
2020年12月4日,诺和诺德向FDA提交了司美格鲁肽2.4mg每周皮下注射1次用于减肥的上市申请。
2021年4月,获国家食品药品监督管理局(NMPA)批准,用于治疗成人2型糖尿病及降低T2DM合并心血管疾病患者的心血管不良事件风险。
2021年12月3日,被纳入《国家基本医疗保险、工伤保险和生育保险药品目录(2021年)》。
药品成分
活性成份:司美格鲁肽(通过基因重组技术,利用酿酒酵母细胞生产的人胰高血糖素样肽-1 (GLP-1)类似物)。1ml注射液中含有1.34mg司美格鲁肽。每支预填充注射笔含有司美格鲁肽2mg,置于1.5ml溶液中。
化学名称:Nε26[(S)-(22,40-二羧酸-10,19,24-三氧代-3,6,12,15-四氧杂-9,18,23-三氮杂四十烷-1-酰基)][Aib8,Arg34]GLP-1-(7-37)肽
化学结构式:
分子式:C187H291N45O59
分子量:4113.58g/mol
辅料:磷酸氢二钠二水合物、丙二醇、苯酚、盐酸(用于调节pH值)、氢氧化钠(用于调节pH值)和注射用水。本品以苯酚作为抑菌剂,每100ml本品中加入苯酚0.550g。
适应症
本品适用于成人2型糖尿病患者的血糖控制:在饮食控制和运动基础上,接受二甲双胍和/或磺脲类药物治疗血糖仍控制不佳的成人2型糖尿病患者。
适用于降低伴有心血管疾病的2型糖尿病成人患者的主要心血管不良事件(心血管死亡、非致死性心肌梗死或非致死性卒中)风险。
用法用量
用法
本品应每周注射一次,可在一天中任意时间注射,无需根据进餐时间给药。
本品经皮下注射给药,注射部位可选择腹部、大腿或上臂。改变注射部位时无需进行剂量调整。本品不可静脉或肌肉注射 。
如有必要,可以改变每周给药的日期,只要两剂间隔至少2天(>48小时)即可。在选择新的给药时间后,应继续每周给药一次。
有关给药的更多信息见使用和其他操作的特别注意事项。
用量
司美格鲁肽的起始剂量为0.25mg每周一次。4周后,应增至0.5mg每周一次。在以0.5mg每周一次治疗至少4周后,剂量可增至1mg每周一次,以便进一步改善血糖控制水平。本品0.25mg并非维持剂量。不推荐每周剂量超过1mg。
当司美格鲁肽用于联合已有的二甲双胍治疗时,可维持当前二甲双胍剂量不变。
当本品用于联合已有的磺脲类药物治疗时,应考虑减少磺脲类药物的剂量,以降低低血糖的风险(见【不良反应】和【注意事项】)。
无需为调整本品剂量而进行自我血糖监测。但是,当开始使用本品与磺脲类药物联合治疗时,则可能需要自我监测血糖,以调整磺脲类药物的剂量,从而降低低血糖的风险(见【注意事项】)。
遗漏用药
如发生遗漏用药,应在遗漏用药后5天内尽快给药。如遗漏用药已超过5天,则应略过遗漏的剂量,在正常的计划用药日接受下一次用药。在每种情况下,患者均应恢复每周一次的规律给药计划。
注意事项
本品不得用于1型糖尿病患者或用于治疗糖尿病酮症酸中毒。本品并非胰岛素的替代品。
尚无本品在纽约心脏病学会(NYHA)分级IV级的充血性心力衰竭患者中的使用经验,因此不推荐此类患者使用本品。
胃肠道反应:使用GLP-1受体激动剂可能与胃肠道不良反应有关。
急性胰腺炎:曾有使用GLP-1受体激动剂后发生急性胰腺炎的情况。如果怀疑胰腺炎,应停用本品;如确诊为胰腺炎,不应再使用本品进行治疗。有胰腺炎病史的患者应慎用本品。
低血糖:接受本品联合磺脲类药物或胰岛素治疗的患者发生低血糖的风险可能会增高。开始本品治疗后,可以通过减少磺脲类药物或胰岛素的剂量来降低低血糖风险。
糖尿病视网膜病变:在接受胰岛素和司美格鲁肽治疗并伴有糖尿病视网膜病变的患者中,观察到发生糖尿病视网膜病变并发症的风险增加。已有糖尿病视网膜病变的患者在接受胰岛素治疗的基础上加用本品时应慎重。
甲状腺C细胞肿瘤风险:目前尚不清楚司美格鲁肽是否会引起人类甲状腺C细胞肿瘤,包括甲状腺髓样癌(MTC)。本品禁用于有MTC个人既往病史或家族病史的患者,或MEN 2患者。应告知患者使用本品可能的MTC风险,以及甲状腺肿瘤的症状(例如颈部肿块、吞咽困难、呼吸困难、持续性声音嘶哑)。
急性肾损害:在使用GLP-1受体激动剂治疗的患者中,已有关于急性肾损害和慢性肾衰竭加重的上市后报告,这些病例有时可能需要血液透析。这些事件中有些发生在没有已知的基础肾病的患者中。大多数报告的事件发生在既往出现过恶心、呕吐、腹泻或脱水的患者中。对于报告重度胃肠道不良反应的患者,应在开始使用本品或进行剂量递增时监测其肾功能。
过敏反应:使用GLP-1受体激动剂曾有报告严重的过敏反应(如速发过敏反应、血管性水肿)。如发生过敏反应,应停用本品;立即给予标准治疗,并监测患者直至体征和症状消退。切勿用于既往对本品过敏的患者(见【禁忌】)。
其他GLP-1受体激动剂有引起速发过敏反应和血管性水肿的报告。既往曾对另一种GLP-1受体激动剂有血管性水肿或速发过敏反应史的患者应慎用本品,因为尚不明确此类患者接受本品治疗后是否更容易发生速发过敏反应。
钠含量:本品每剂含钠小于1mmol(23mg),即基本上“无钠”。
对驾驶和机械操作能力的影响:司美格鲁肽对驾驶车辆或使用机器的能力没有影响或影响很小可以忽略不计。当与磺脲类药物或胰岛素联合使用时,应建议患者在驾驶和使用机器时采取预防措施,避免发生低血糖(见【注意事项】)。
相关推荐
-

- 刘强东花180亿买了个德国零售新平台
-
7月31日,京东在港交所发布公告称,决定通过全资间接附属公司(出价方),收购德国最大的消费类电子产品集团CECONOMY,估值约22亿欧元,折合人民币超180亿元。Ceconomy是德国电子产品零售商,擅长销售电脑、手机等3C产品,旗下拥有...
-
2025-08-03 22:43 阿輝
- 减少手机号泄露风险!工信部:700号段将成为“隐私号”专用码号资源
-
今后在拨打或接听电话时,如果你看到15位长的“700XXXXXXXXXXXX”号码,即可认定此次通信使用了号码保护服务,对方将看不到你的实际号码。工信部通知7月2日,工信部官网发布《关于开展号码保护服...
-
- 减重专家破解减肥十大谣言,你中了几招?
-
谣言1:节食是最快的减肥方法 辟谣:节食会导致肌肉流失、基础代谢率下降,容易反弹。长期低热量饮食还可能引发营养不良、内分泌紊乱。科学减重应保持合理热量缺口(每日300-500大卡),均衡饮食。谣言2:不吃碳水才能瘦 辟谣...
-
2025-05-27 20:39 阿輝
-

- 耐克时隔六年将恢复在亚马逊平台上销售
-
财联社5月22日讯:美国关税政策对零售业的影响正在逐步显现。美运动用品巨头耐克宣布,将提高商品的价格,并恢复在亚马逊的直接销售。由于自海外采购的成本大幅升高,耐克将全面调整产品价格,不同商品的价格涨幅有所不同。据一名知情人士透露,售价超过1...
-
2025-05-22 23:31 阿輝
-

- 国产操作系统加速崛起!中国操作系统市场规模或达250亿元
-
人民财讯5月19日电,近年来,国产操作系统加速崛起,核心业务系统升级进入深水区,中国操作系统厂商正通过新一轮信息技术创新破局。最新数据显示,2025年,中国操作系统市场增速加快,市场规模预计将达到250亿元。记者了解到,目前,多个国产操作系...
-
2025-05-20 21:47 阿輝
-

- 市场监管总局十项措施,整治“内卷式”竞争
-
...
-
2025-05-20 21:30 阿輝
-

- 京东、美团、饿了么等外卖平台,被中央5部门约谈!
-
近日,市场监管总局会同中央社会工作部、中央网信办、人力资源社会保障部、商务部,针对当前外卖行业竞争中存在的突出问题,约谈京东、美团、饿了么等平台企业。要求相关平台企业严格遵守《中华人民共和国电子商务法》《中华人民共和国反不正当竞争法》《中华...
-
2025-05-14 22:51 阿輝
- 苹果宣布降价,涉及苹果iPhone16Pro,iPhone16ProMax
-
5月10日,有消息称苹果向渠道商发布了调价通知,苹果iPhone16ProMax所有容量版本降价160美元,(折合人民币1313.06元);而iPhone16Pro的128GB版本降价1...
-

- 网爆:“刘强东穿猪猪侠T恤现身日本”被偶遇
-
5月10日,有网友在日本东京街头偶遇京东创始人刘强东,照片中的他身着一件猪猪侠与京东外卖联名的白色T恤,T恤正面印有猪猪侠背着京东外卖箱的可爱图案,背后则印着京东外卖的二维码,该照片迅速在网络上引发广泛关注与讨论。今年4月,刘强东曾亲自体...
-
2025-05-11 17:41 阿輝
- 发改委推出3万亿元优质项目,支持民企参与
-
国家发展改革委副主任郑备介绍,民营经济促进法全文贯穿了平等对待、公平竞争、同等保护、共同发展的原则,不仅在总则,而且在公平竞争、投资融资促进、科技创新、法律责任等章节中,都予以了充分体现。落实法律要求...
欢迎 你 发表评论:
- 一周热门
- 搜索












 浙公网安备 33032402001686号
浙公网安备 33032402001686号